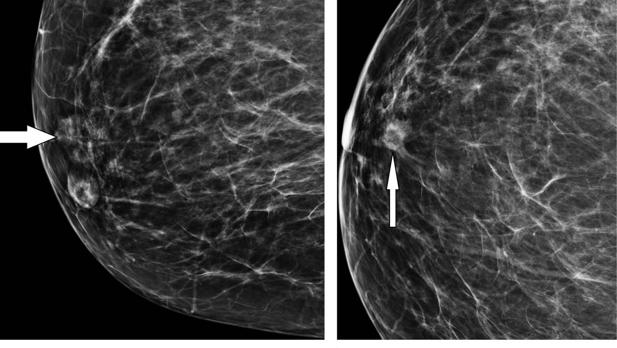
Expertos de 40 hospitales españoles han demostrado en un ensayo clínico que añadir un segundo anticuerpo monoclonal al tratamiento estándar aplicado tras la cirugía en tumores precoces HER2 positivos, aumenta las posibilidades de curación del cáncer de mama
Dicha participación incluye a hospitales de 12 comunidades autónomas, con Andalucía y Cataluña a la cabeza con seis centros cada una, seguidas de Madrid (5), Comunidad Valenciana (4), Galicia (2), País Vasco (2). También han colaborado con un hospital Aragón, Canarias, Castilla León, Murcia, Castilla La Mancha y Cantabria. GEICAM ha sido el tercer grupo con mayor reclutamiento según la Organización Internacional de Grupos Académicos de Investigación en Cáncer de Mama, Breast International Group (BIG).
«La relevancia de ensayo clínico demuestra que España mantiene su papel destacado en la investigación clínica de tumores HER2 positivo. Tras varios estudios esenciales con estos mismos fármacos en fases avanzadas, los datos ahora indican que su uso en fases iniciales antes y después de la cirugía avalan su potencial para buscar la curación», ha apostillado el oncólogo del Hospital Virgen del Rocío de Sevilla, Manuel Ruíz Borrego.
Por tanto, el ensayo clínico ha alcanzado su objetivo primario al demostrar que un tratamiento adyuvante (después de la cirugía) basado en la combinación de pertuzumab, trastuzumab y quimioterapia logra una reducción estadísticamente significativa del riesgo de recaída de enfermedad invasiva o fallecimiento en mujeres con cáncer de mama precoz HER2+ frente a trastuzumab y quimioterapia sola.
Seguridad del tratamiento
Además, el perfil de seguridad de la terapia con pertuzumab fue consistente con lo que ya se conocía por estudios previos, y no se identificaron nuevos indicios de seguridad. La combinación de Pertuzumab y quimioterapia ya está autorizada como terapia neoadyuvante (antes de la cirugía) en pacientes con cáncer de mama precoz HER2+ en más de 75 países, tras las aprobaciones de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) y de la Agencia Americana del Medicamento (FDA, por sus siglas en inglés). En Estados Unidos, el tratamiento está actualmente disponible bajo el programa de aprobación acelerada que concede la FDA.
Este medicamento es una terapia personalizada que actúa sobre el receptor HER2, una proteína que se encuentra en cantidades elevadas en la parte exterior de las células tumorales HER2 positivo. Los resultados completos del estudio, denominado ‘Aphinity’, serán presentados en la próxima Reunión Anual de la Sociedad Americana de Oncología Clínica (ASCO, por sus siglas en inglés), que tendrá lugar en Chicago entre los días 2 y 6 de junio.
Fuente: La sexta