Eva Ciruelos aparece en más de medio centenar de estudios sobre cáncer de mama sólo en la base de datos de ensayos clínicos de EE UU. Como presidenta de Solti (un grupo académico de investigación clínica en este tipo de tumores) conoce el nivel que España tiene en este área y destaca el buen papel que se desempeñan nuestros investigadores y centros.
Con la llegada de la inmunoterapia en el cáncer de mama triple negativo, ¿se está más cerca de tener bajo control este tipo de tumor?
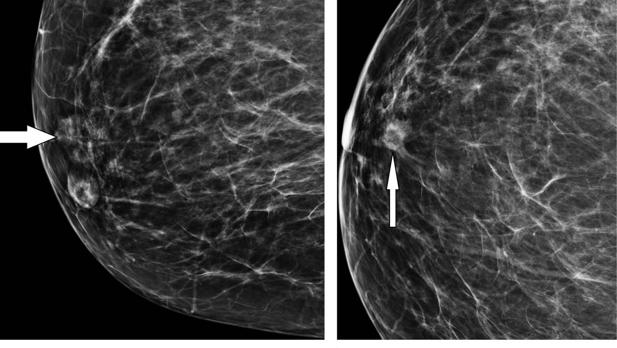
-Sí, claro. Hasta ahora el triple negativo era el subtipo con menos opciones terapéuticas, pero ahora ya contamos con una opción válida y segura, como la inmunoterapia. No se trata de que sea para todas las de este grupo, sino para un 40% de las mismas, que tiene un marcador PDL-1 positivo del que nos vamos a beneficiar. Por lo tanto, yo diría que sí nos vamos acercando más a que cualquier paciente de cáncer de mama tenga opciones terapéuticas esperanzadoras.
–¿Qué papel ha jugado España en los ensayos clínicos que han demostrado la efectividad de este nuevo abordaje?
-En nuestro país han participado nueve centros. Puedo decir con seguridad que los hospitales españoles contribuyen muy notablemente en los estudios clínicos con un nivel de reclutamiento y de calidad muy alto, estamos casi siempre posicionados entre los cinco primeros países en cuanto a lo primero. Resulta un orgullo que cuando sale una noticia de este tipo, que puede ser un avance positivo o negativo, los investigadores lo agradecen por la recogida de datos. También lo valoran las pacientes, porque son las primeras al poder beneficiarse de estos avances dentro de los estudios.
Al final, la realización de ensayos clínicos es un quid pro quo para todas las partes, ¿cierto?
-Exactamente. Pero no sólamente ya por los tratamientos, que funcionen bien, porque pueden ir mejor o peor, sino porque el hecho de caer en un ensayo clínico como paciente o como investigador nos hace ver mejor las cosas. Podemos elaborar mejores seguimientos, estudiar con sumo cuidado los informes radiológicos, analizar mejor las muestras tumorales con biomarcadores, hacer un seguimiento óptimo de las medicaciones concomitantes que toma el paciente… Los investigadores no están acostumbrados a tratar en el día a día de la clínica y también aprenden mucho de esta experiencia. Ya no sólo se trata de los buenos datos del estudio –que ha visto la luz en «The New England Journal of Medicine»–, y que es una alegría, sino por la exigencia que la investigación precisa en el seguimiento de las mujeres incluidas.
El trabajo pone de manifiesto la utilidad de la combinación de la molécula atezolizumab –de Roche– y quimioterapia eleva en año y medio la media de la supervivencia, ¿en qué consiste?
-Se trataba de comparar la eficacia de un nuevo abordaje –en este caso un fármaco– con lo que hasta ahora se emplea de forma estándar en estas pacientes. Se combina el atezolizumab con una quimioterapia basada en taxanos muy conocido, en concreto el nab-paclitaxel, que no tiene tóxicos y llega muy bien a los tejidos a los que se busca tratar.
Además, demuestran que es eficaz en un grupo concreto de pacientes. ¿Esto es lo que hoy los expertos denominan medicina personalizada?
-Sí, en aquellas con expresión positiva PDL-1. Se trata de un marcador que se mide con diferentes anticuerpos en unas condiciones concretas en las muestras tumorales. Esto se ha aprendido a hacer muy bien en otros tipos de cáncer candidatos a inmunoterapia, como el de pulmón o melanoma. En el estudio, más o menos el 40% de las pacientes incluidas tenían ese marcador positivo. Este proceso es fácil de hacer, no es caro y tenemos experiencia previa para realizarlo.
Fuente: La Razón